Curva de valoracion
Es una gráfica del pH en función del volumen de una disolución titulante (generalmente una base o un ácido) que se va agregando poco a poco a otra disolución de concentración conocida.
Sirve para:
-
Determinar la concentración de un ácido o una base.
-
Identificar el punto de equivalencia.
-
Elegir el indicador ácido-base adecuado.

🧪 ¿Qué ocurre durante una valoración?

Si se valora un ácido con base
Al inicio, el pH es bajo (ácido).
-
A medida que se agrega la base, el ácido se va neutralizando.
-
El pH aumenta poco a poco.
-
Cerca del punto de equivalencia, el pH cambia muy rápidamente.
-
Después del punto de equivalencia, la solución se vuelve básica.
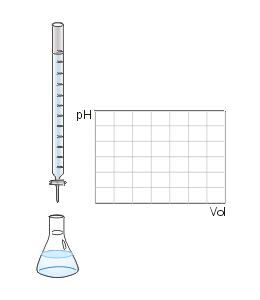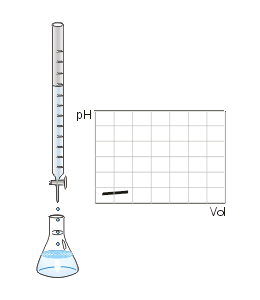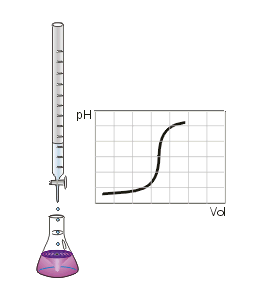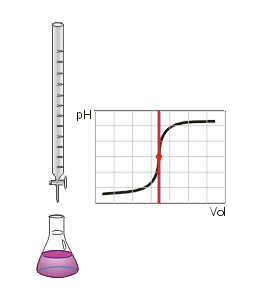
🎯 Punto de equivalencia
Es el punto donde:
moles de ácido=moles de base
En ese momento ocurre la neutralización completa:
ácido+Base → Sal+Agua
En la curva, este punto corresponde al salto brusco de pH.
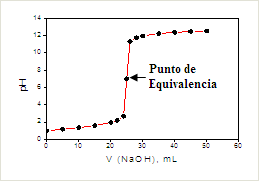




Ácido débil – Base fuerte
Ejemplo: ácido acético con NaOH
-
pH inicial más alto
-
Punto de equivalencia en pH mayor que 7
-
Aparece una zona amortiguadora (buffer) antes del punto de
Ácido fuerte – Base fuerte
Ejemplo: HCl con NaOH:
-
pH inicial muy bajo
-
Punto de equivalencia en pH = 7
-
Cambio de pH muy abrupto
Base débil – Ácido fuerte
Ejemplo: amoníaco con HCl
-
pH inicial alto
-
Punto de equivalencia menor que 7
MOL DE TITRAND
En una titulación, hay dos sustancias principales:
Titulante → la solución de concentración conocida (por ejemplo, NaOH).
Titrando (o analito) → la solución de concentración desconocida que queremos analizar (por ejemplo, HCl).
El mol de titrando es simplemente la cantidad de sustancia que hay del analito, expresada en moles, y que va a reaccionar con el titulante.
